傳統的TIL細胞療法是指從患者自身的腫瘤組織中(zhōng)采集并分(fēn)離出具(jù)有(yǒu)特異性識别腫瘤細胞抗原能(néng)力的T淋巴細胞,在體(tǐ)外通過白介素-2快速活化和擴增後再回輸到患者體(tǐ)内, 最終實現對腫瘤的裂解和殺傷效果的一種細胞療法。
TILs主要包括T細胞、巨噬細胞、NK細胞和樹突細胞等,在TILs亞群中(zhōng),起到正向調節免疫應答(dá)的免疫細胞包括CD4+Th1細胞、CD8+細胞毒性T細胞、NK細胞、巨噬細胞M1型和樹突細胞DC1型等,可(kě)發揮很(hěn)好的抗腫瘤細胞免疫應答(dá)。
另外,因TILs來自腫瘤組織,具(jù)有(yǒu)很(hěn)強的腫瘤歸巢特性,對腫瘤細胞具(jù)有(yǒu)良好的靶向作(zuò)用(yòng),與其它免疫療法(例如CAR-T、PD-1/PD-L1抗體(tǐ))相比,TIL具(jù)有(yǒu)多(duō)靶點、腫瘤趨向和浸潤能(néng)力強、副作(zuò)用(yòng)小(xiǎo)等優勢,是實體(tǐ)瘤治療的理(lǐ)想選擇,前景廣闊。
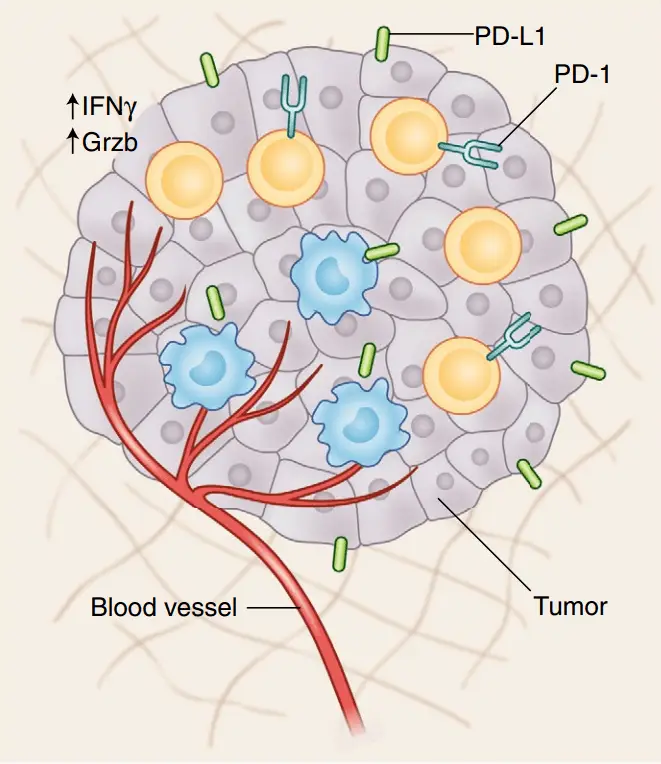
細胞療法的先驅
TIL療法治療實體(tǐ)瘤療效顯著:
早在1982年,免疫學(xué)先驅Steven Rosenberg教授報導從多(duō)個小(xiǎo)鼠腫瘤模型中(zhōng)分(fēn)離出TIL[3];1985年,他(tā)又(yòu)在《新(xīn)英格蘭醫(yī)學(xué)雜志(zhì)》(NEJM)報道了IL-2治療轉移性癌症的成果[4]。此時,人們已認識到IL-2可(kě)促進T細胞的增殖和功能(néng),從腫瘤組織分(fēn)離出TIL細胞,在體(tǐ)外經IL-2擴增後再輸回患者體(tǐ)内進行腫瘤治療成為(wèi)可(kě)能(néng)。
1988年,NEJM發表了TIL療法的最早臨床數據,同樣來自于Rosenberg團隊。15例未接受過IL-2治療的轉移性黑色素瘤患者,經TIL治療後達到了60%的客觀緩解率(ORR)[5]。TIL療法證實在實體(tǐ)瘤中(zhōng)具(jù)有(yǒu)療效。随後,Rosenberg實驗室的Patrick Hwu改進了TIL治療方案,在接受TIL回輸前,先使用(yòng)化療藥物(wù)(環磷酰胺和氟達拉濱)清除患者體(tǐ)内的淋巴細胞,這一預處理(lǐ)方案顯著延長(cháng)了TIL療法的維持時間,增強了抗腫瘤效果,并成為(wèi)此後細胞療法的标準操作(zuò)。
2011年,Rosenberg确認了自體(tǐ)TIL細胞療法可(kě)以在轉移性黑色素瘤患者中(zhōng)介導持久的完全反應[6]。招募的93例患者中(zhōng),20例患者腫瘤完全消退,達到完全緩解(CR),全部患者的3年和5年生存率分(fēn)别為(wèi)36%和29%,20例CR患者的3年和5年生存率分(fēn)别為(wèi)100%和93%。TIL療法在晚期黑色素瘤中(zhōng)的數據在當時引起了極大的關注,實際上TIL療法在多(duō)種癌症中(zhōng)均顯示出良好的療效。
多(duō)種實體(tǐ)瘤中(zhōng)展現療效
據吉濤生物(wù)創始人劉天津介紹,TIL療法已在治療宮頸癌、子宮内膜癌、黑色素瘤、膽管細胞癌、卵巢癌、胰腺癌等臨床試驗中(zhōng)取得令人可(kě)喜的療效數據。TIL療法是一個适應症覆蓋面非常廣的療法,對于多(duō)種類型的實體(tǐ)腫瘤都能(néng)産(chǎn)生不錯療效。而吉濤生物(wù)新(xīn)型的DC-TIL療法将突破傳統制備上的細胞數量,利用(yòng)新(xīn)型誘導技(jì )術和激活方式讓戰鬥的細胞數值達到2400億單位量。
TIL療法治療實體(tǐ)瘤
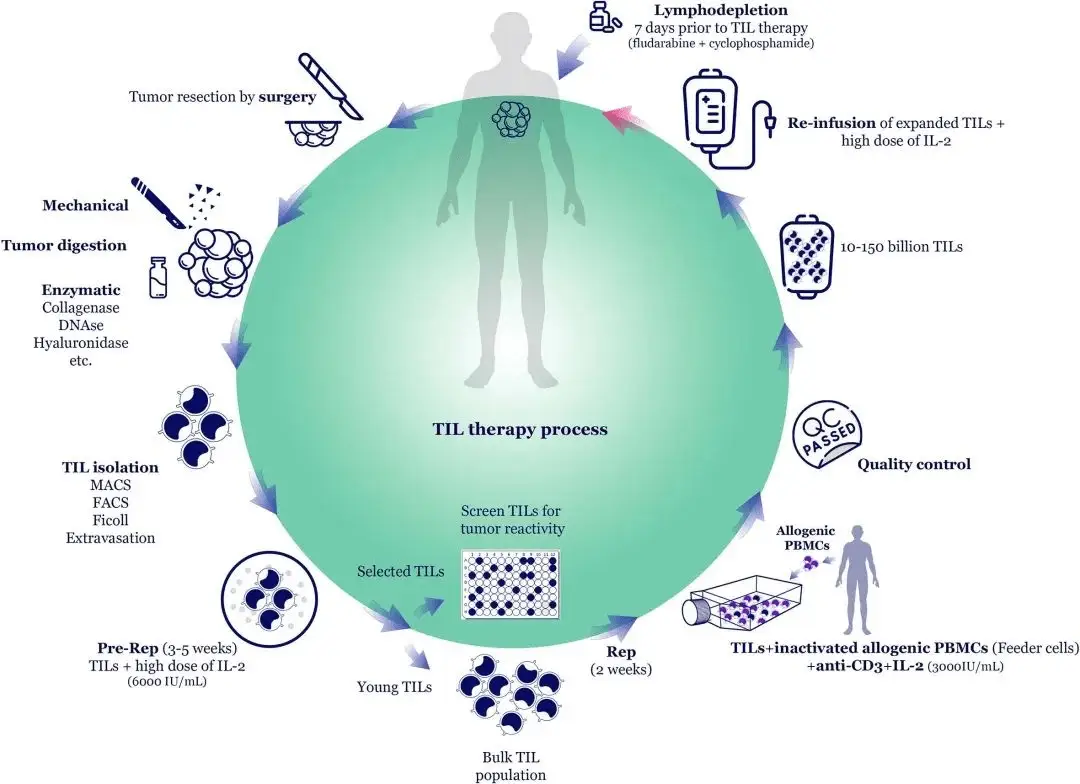
傳統TIL療法流程
TIL療法在實體(tǐ)瘤中(zhōng)取得的療效基于其具(jù)有(yǒu)優勢:
靶向性強:來自于腫瘤組織的TIL主要由效應記憶T細胞(Tem)組成,表面表達的趨化因子受體(tǐ)(如CCR5、CXCR3)聯合多(duō)種腫瘤特異性TCR,在TIL輸注後,可(kě)以準确靶向腫瘤新(xīn)生抗原;
腫瘤浸潤能(néng)力強:TIL細胞來自腫瘤,腫瘤趨化因子受體(tǐ)高表達,合适的趨化因子受體(tǐ)系統,使得TIL回輸後可(kě)更好地浸潤腫瘤組織;
安(ān)全窗口高:天然TCR識别,耐受高達10E11級的回輸劑量,安(ān)全窗口非常寬,僅識别腫瘤細胞抗原,不會靶向自身正常細胞,臨床上顯示良好的安(ān)全性;
療效持久:TIL細胞中(zhōng)記憶性T細胞比例高,是非選擇的腫瘤特異性殺傷T細胞,靶向多(duō)種抗原,可(kě)克服因靶點丢失引起的複發問題。2012年接受TIL療法的幸存者Melinda,目前已成功存活11年。
技(jì )術創新(xīn)對突破TIL療法
技(jì )術壁壘極為(wèi)重要
目前,TIL療法已形成了一個标準治療流程,其中(zhōng)注入的DC細胞-樹突狀細胞是近年來吉濤生物(wù)新(xīn)興的一種生物(wù)治療惡性腫瘤的方法,已經越來越受到腫瘤專家的關注和認可(kě)。它主要是通過在體(tǐ)外短時間内誘導培養出大量的帶有(yǒu)腫瘤抗原的樹突狀細胞,準确“瞄準”并殺傷癌細胞。
不僅如此,它還能(néng)在患者體(tǐ)内誘發免疫記憶,使患者獲得長(cháng)期的抗癌效應。通過DC細胞和TIL細胞的雙重結合,共培養時自體(tǐ)的DC細胞通過MHC分(fēn)子遞呈腫瘤抗原給TIL細胞,将會規模化擴增新(xīn)生抗原TIL細胞(GT-001),簡而言之即特異性殺傷腫瘤的有(yǒu)效細胞增多(duō),更加準确化攻擊。

“我們的TIL細胞具(jù)有(yǒu)更高的腫瘤特異性”,據劉博介紹,當TIL細胞遇到腫瘤細胞刺激後,能(néng)更好的與腫瘤細胞反應,實現在體(tǐ)内的二次、三次擴增,并能(néng)夠實現在患者體(tǐ)内不用(yòng)額外輸注就能(néng)很(hěn)好的進行擴增。
目前,全球已上市多(duō)款細胞治療産(chǎn)品,從銷售情況來看并沒有(yǒu)達到理(lǐ)想的預期。影響細胞療法應用(yòng)的主要因素有(yǒu)三個方面:一是療效本身的不确定性,主要是能(néng)否治愈以及複發的挑戰;二是價格因素,已上市細胞療法都是定制化産(chǎn)品,高昂的生産(chǎn)成本導緻藥品售價過高;三是患者數量不确定,各種因素會影響到最終适合接受細胞療法的人群數量。
事物(wù)的發展規律都是遵循前進性和曲折性必存。隻要腳踏實地堅持做自己認為(wèi)對的事,穩紮穩打,市場會自動進行篩選。當一些追求熱點,技(jì )術不太紮實的團隊被排除在市場之外,留下具(jù)有(yǒu)更好技(jì )術含量、具(jù)有(yǒu)創新(xīn)力和執行力的團隊,對于整個行業的健康發展總體(tǐ)是有(yǒu)利的。在曆史的洪流面前,任何可(kě)能(néng)都是存在的,相信在TIL療法領域也一定會有(yǒu)收獲!
吉濤生物(wù)
上海吉濤公(gōng)司總部及研發中(zhōng)心位于上海,是國(guó)家高新(xīn)技(jì )術企業和國(guó)家認可(kě)的醫(yī)學(xué)檢驗機構,也是上海市靜安(ān)區(qū)重點大數據企業。公(gōng)司準确定位于防癌抗衰老領域的新(xīn)技(jì )術開發、癌症準确預防及治療方案制定、抗衰老産(chǎn)品研發等。吉濤醫(yī)學(xué)作(zuò)為(wèi)上海吉濤的醫(yī)學(xué)服務(wù)平台,為(wèi)醫(yī)院及用(yòng)戶提供準确醫(yī)療及抗衰老服務(wù)。
公(gōng)司專注于免疫細胞、幹細胞治療技(jì )術的開發,以及癌症早期診斷、早期幹預新(xīn)技(jì )術的開發與應用(yòng)。公(gōng)司開發了基于 ctDNA 甲基化檢測的腫瘤早期診斷平台,以及用(yòng)于準确治療的免疫細胞、幹細胞的存儲和細胞制備平台,擁有(yǒu)研發團隊,是中(zhōng)國(guó)醫(yī)藥生物(wù)技(jì )術協會會員單位。
參考文(wén)獻:
[1]Chen X, Li P, Tian B and Kang X (2022) Serious adverse events and coping strategies of CAR-T cells in the treatment of malignant tumors. Front. Immunol. 13:1079181.
[2]Hernández-López A, Téllez-González MA, Mondragón-Terán P, Meneses-Acosta A. Chimeric Antigen Receptor-T Cells: A Pharmaceutical Scope. Front Pharmacol. 2021 Aug 20;12:720692.
[3]berlein TJ, Rosenstein M, Rosenberg SA. Regression of a disseminatedsyngeneic solid tumor by systemic transfer of lymphoid cells expanded ininterleukin 2. J Exp Med. 1982;156(2):385–97
[4]Rosenberg SA, et al. 1985.Observations on the systemic administration of autologous lymphokine-activatedkiller cells and recombinant interleukin-2 to patients with metastatic cancer.N Engl J Med 313(23):1485–1492.





